jCyte, Inc., una empresa biotecnológica pionera dedicada a preservar y restaurar la visión en pacientes con retinosis pigmentaria (RP) y otros trastornos degenerativos de la retina, se complace en anunciar el resultado exitoso de su reunión previa a la fase 3 Tipo B con la Administración de Alimentos y Medicamentos de EE. UU. (FDA) celebrada el 16 de enero de 2024. Además, la compañía se está preparando para comenzar su prueba fundamental en EE. UU. para jCell en la segunda mitad de 2024.
John Sholar, director ejecutivo de jCyte, expresó su satisfacción con la revisión por parte de la FDA del diseño del ensayo clínico de fase 2/3 planificado, incluida la aprobación por parte de la FDA del criterio de valoración primario y las dos dosis de jCell que se incluirán en el estudio. Sholar también se mostró encantado con las respuestas de la FDA a la descripción de jCyte de su programa CMC. «Estamos satisfechos con las actas de la reunión de tipo B, que nos permiten avanzar con el ensayo fundamental de EE. UU. Se espera que la inscripción comience en la segunda mitad de este año y se compartirá más información cuando sea apropiado».
Paul Sieving, MD, PhD, profesor de oftalmología Neil y MJ Kelly en la Facultad de Medicina de UC Davis y ex director del Instituto Nacional del Ojo (NEI) en el Instituto Nacional de Salud (NIH), se mostró entusiasmado con la noticia y declaró: «Estoy ansioso por ver que esta prometedora terapia se convierta en un ensayo fundamental en los EE. UU.».
Henry Klassen, MD, PhD, cofundador y presidente de jCyte, reconoció la importancia de este logro en la búsqueda de un tratamiento para pacientes con retinosis pigmentaria. «Este es un paso importante en nuestro largo viaje para tratar la RP. Estoy inmensamente orgulloso de nuestro equipo. Se necesitó mucho trabajo duro, innovación y perseverancia para alcanzar este hito. Todos estamos ansiosos por seguir adelante y hacer llegar este tratamiento a los pacientes».
Acerca de jCyte, Inc.
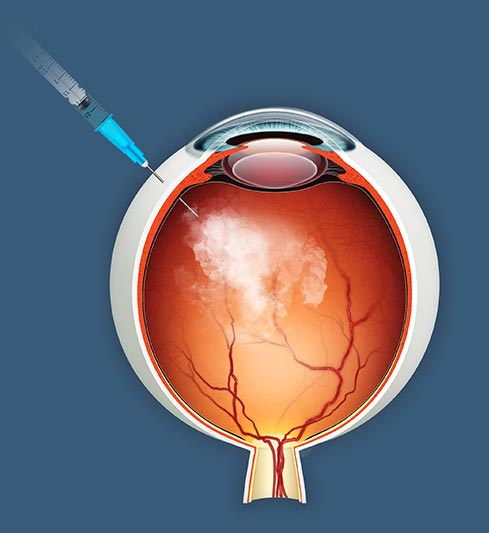
jCyte, Inc. es una empresa de biotecnología en fase clínica centrada en el desarrollo de su primera terapia celular alogénica, jCell, para la retinosis pigmentaria (RP) y otros trastornos degenerativos de la retina. El tratamiento ha recibido la designación de Terapia Avanzada de Medicina Regenerativa (RMAT) de la FDA y se administra como una inyección intravítrea mínimamente invasiva. Actualmente no existen terapias aprobadas por la FDA para más del 99% de los pacientes con RP. La compañía es pionera en una nueva era de terapias regenerativas para abordar las importantes necesidades médicas insatisfechas de los pacientes que padecen un amplio conjunto de enfermedades degenerativas de la retina. Para obtener más información, visite www.jcyte.com.
Contactos
jCyte, Inc.
Víctor Chao
, Vicepresidente de Operaciones Comerciales y Estrategia
Media@jcyte.com
Puedes encontrar aquí el artículo orginal